 Sulla base delle evidenze scientifiche disponibili ad oggi non è dimostrato che i pazienti pediatrici che in passato hanno avuto diagnosi di malattia di Kawasaki siano esposti ad un rischio maggiore rispetto agli altri bambini di contrarre SARS-CoV-2, né di presentare una recidiva di malattia di Kawasaki. Tuttavia, recenti pubblicazioni scientifiche descrivono una sindrome infiammatoria acuta multisistemica in età pediatrica e adolescenziale, associata a positività per il SARS-CoV-2 o presenza di anticorpi anti SARS-CoV-2. Questa sindrome sembrerebbe condividere alcune caratteristiche cliniche con la malattia di Kawasaki ma, secondo le indicazioni dell’European Centre for Disease Prevention and Control (ECDC) e della World Health Organization (WHO), si tratta di una forma clinica che va differenziata dalla malattia di Kawasaki e che è ancora in via di definizione.
Sulla base delle evidenze scientifiche disponibili ad oggi non è dimostrato che i pazienti pediatrici che in passato hanno avuto diagnosi di malattia di Kawasaki siano esposti ad un rischio maggiore rispetto agli altri bambini di contrarre SARS-CoV-2, né di presentare una recidiva di malattia di Kawasaki. Tuttavia, recenti pubblicazioni scientifiche descrivono una sindrome infiammatoria acuta multisistemica in età pediatrica e adolescenziale, associata a positività per il SARS-CoV-2 o presenza di anticorpi anti SARS-CoV-2. Questa sindrome sembrerebbe condividere alcune caratteristiche cliniche con la malattia di Kawasaki ma, secondo le indicazioni dell’European Centre for Disease Prevention and Control (ECDC) e della World Health Organization (WHO), si tratta di una forma clinica che va differenziata dalla malattia di Kawasaki e che è ancora in via di definizione.
L’ISS, al riguardo, ha pubblicato il RAPPORTO COVID-19 “Indicazioni ad interim su malattia di Kawasaki e sindrome infiammatoria acuta multisistemica in età pediatrica e adolescenziale nell’attuale scenario emergenziale da infezione da SARS-CoV-2” , elaborato da un gruppo interdisciplinare di esperti, coordinato da Domenica Taruscio. Il Rapporto è un documento operativo di sanità pubblica che fornisce indicazioni essenziali e raccomandazioni per affrontare e gestire questa sindrome pediatrica e adolescenziale ancora in via di completa definizione.
“Si tratta di un evento grave, ancorché raro, che merita tutta l’attenzione dei pediatri, degli infettivologi, dei reumatologi, dei cardiologici e degli altri professionisti della salute, soprattutto considerando l’associazione con la pandemia da COVID-19 tuttora in corso – afferma Domenica Taruscio, Direttore del Centro Nazionale Malattie Rare (ISS) e coordinatrice del Gruppo di lavoro “COVID-19 e Malattie rare” – E’ infatti importante identificare precocemente i pazienti, ricoverarli tempestivamente ed effettuare l’accertamento diagnostico accurato per avviarli al trattamento appropriato”.
La malattia di Kawasaki
La malattia di Kawasaki è una vasculite sistemica che colpisce prevalentemente i bambini di età inferiore a 5 anni e la cui prognosi dipende essenzialmente dal coinvolgimento delle arterie coronarie. Ha un’incidenza in Italia di circa 14 su 100.000/anno in bambini sotto i 5 anni, con un numero di casi di circa 450/anno calcolato sulla base delle dimissioni ospedaliere. I sintomi sono febbre (≥38°C), congiuntivite bilaterale senza secrezioni, arrossamento delle labbra e della mucosa orale, eruzione cutanea e linfoadenopatia cervicale monolaterale, che possono anche non essere tutti presenti contemporaneamente. E’importante che il bambino con questi sintomi venga rapidamente valutato dal pediatra e portato in ospedale per effettuare gli accertamenti clinici e laboratoristici. Se la diagnosi viene confermata, si deve iniziare la terapia farmacologia appropriata nei tempi previsti dalle linee guida. Pertanto, l’appropriatezza e la tempestività della diagnosi incidono in modo considerevole sulla prognosi. Non ci sono al momento evidenze che il trattamento della malattia di Kawasaki debba essere modificato in epoca di pandemia COVID-19 rispetto alle linee guida esistenti.
I dati epidemiologici della malattia di Kawasaki suggeriscono un’eziologia infettiva, sebbene l’agente causale non sia ancora stato identificato. Non è stabilita, al momento, un’associazione con l’infezione da SARS-CoV-2. In particolare non è possibile al momento attuale verificare se il numero dei soggetti affetti sia aumentato quest’anno, in concomitanza con l’epidemia da COVID-19.
La sindrome infiammatoria acuta multisistemica
L’ECDC ha pubblicato, lo scorso 15 maggio, un Rapid Risk Assessement sulla sindrome infiammatoria multisistemica pediatrica e adolescenziale e l’infezione da SARS-CoV-2, in cui vengono riportati 230 casi sospetti nell’Unione Europea e nel Regno Unito, con due decessi. I soggetti colpiti hanno un’età media di 7-8 anni, fino 16 anni, e hanno presentato interessamento multisistemico grave, a volte con necessità di ricovero in terapia intensiva. Il reale numero di questi soggetti è ancora in fase di valutazione, così come il preciso inquadramento nosologico di questa condizione, attualmente chiamata “sindrome infiammatoria acuta multisistemica”. Dati sia italiani che inglesi dimostrano che lo sviluppo di questa sindrome segue di 2-4 settimane il picco di infezione da SARS-CoV-2, per cui si ipotizza una patogenesi immunomediata e non legata ad un’infezione diretta del virus. Le caratteristiche della sindrome comprendono un’aberrante risposta infiammatoria, con febbre elevata, shock e prevalente interessamento miocardico e/o gastrointestinale. Le opzioni terapeutiche comprendono immunoglobuline, steroidi, farmaci anticitochinici.
Il documento evidenzia che, al momento, pur in assenza di una definizione di caso condivisa a livello europeo, è plausibile una correlazione fra infezione da SARS-CoV-2 e insorgenza della sindrome, pur in presenza di evidenze limitate del nesso di
causalità. “L’esistenza della sindrome è una realtà clinica riconosciuta – va avanti l’esperta – tuttavia è indispensabile una definizione condivisa dei criteri diagnostici, questo permetterà una registrazione sistematica dei casi per valutare la reale incidenza”.
L’infezione da SARS -CoV-2 nei bambini
La reale prevalenza di SARS-CoV-2 nella popolazione pediatrica, così come in quella adulta, non è conosciuta, tuttavia le evidenze scientifiche disponibili ad oggi indicano che l’infezione da SARS-CoV-2 si manifesta nei pazienti pediatrici con un andamento clinico più benigno rispetto all’adulto e con una letalità molto bassa (0,06% nella fascia di età 0-15 anni).
Gli studi effettuati
Un’analisi pubblicata su Pediatrics è stata realizzata in Cina su 2135 bambini con infezione da SARS-CoV-2, diagnosticata o sospetta, segnalati al Chinese Center for Disease Control and Prevention nel periodo tra il 16 gennaio e l’8 febbraio 2020. Di tutti i casi esaminati, 112 (5,2%) hanno sviluppato una forma grave della malattia con una rapida insorgenza di dispnea, ipossia, febbre, tosse e sintomi gastrointestinali, inclusa diarrea. Altri 13 bambini (0,6%) erano in condizioni critiche e hanno manifestato in breve tempo una sindrome da difficoltà respiratoria acuta o insufficienza respiratoria; in questi casi si è potuto anche osservare shock, encefalopatia, danno miocardico o insufficienza cardiaca, coagulopatia e danno renale acuto.
Nell’aprile 2020, i Centers for Disease Control and Prevention (CDC) degli USA hanno pubblicato uno studio sul Morbidity and Mortality Weekly Report, nel quale sono stati analizzati, 149.760 casi risultati positivi per SARS-CoV-2 di cui 2.572 (1,7%) casi avevano un’età inferiore ai 18 anni nel periodo compreso tra il 12 febbraio e il 2 aprile. Nel 73% dei bambini SARS-CoV-2 positivi, era presente almeno uno dei sintomi clinici che sono alla base del sospetto diagnostico (febbre, tosse e dispnea) mentre negli adulti tale percentuale era il 93% (3). Lo stesso documento riportava un tasso di ospedalizzazione in un intervallo stimato tra il 5,7% e il 20%, e di ricovero in terapia intensiva in un range tra lo 0,6% e il 2%. Il tasso di ospedalizzazione era molto maggiore fra i bambini al di sotto di un anno di età (range stimato 15%-62%) mentre nella fascia superiore di età il range stimato era del 4,1-14%. Per 295 casi pediatrici erano disponibili informazioni sanitarie sia sull’ospedalizzazione sia sulle patologie concomitanti. Circa il 77% (28 su 37 casi) dei pazienti ospedalizzati presentavano una o più patologie concomitanti, mentre dei restanti 258 pazienti che non necessitarono di ricovero, 30 (12%) presentavano altre patologie.
In Italia, i dati dell’Istituto Superiore di Sanità (ISS) riportano che al 14 maggio 2020 fra i 29.692 deceduti positivi all’infezione SARS-CoV-2 sono stati rilevati 3 casi relativi alla fascia di età 0-19 anni.
In una casistica, pubblicata su Jama Pediatrics, di 41 pazienti pediatrici spagnoli con confermata infezione da SARS-CoV-2 il 60% (25 casi) ha avuto la necessità di essere ospedalizzato: di questi 4 casi sono stati ricoverati in terapia intensiva e altri 4 hanno avuto necessità di ventilazione assistita.
Secondo il sistema di sorveglianza europeo (The European Surveillance System, TESSy), al 13 maggio 2020, i bambini rappresentano una percentuale molto bassa dei 193.351 casi COVID-19 confermati in Italia; nell’intervallo di età tra i 0-10 anni i casi segnalati sono stati 1,1% e 1% tra 10-19 anni. L’indice di letalità del COVID-19 è quindi pari a 0,06% nella fascia di età 0-15 anni, rispetto al 16,9% nel gruppo di ultra-quindicenni. I 3 bambini deceduti in Italia erano affetti da importanti e gravi patologie (malattia metabolica, cardiopatia, neoplasia).
In una casistica di 100 bambini con tampone positivo al SARS-CoV-2 che hanno fatto accesso al Pronto Soccorso di 17 ospedali italiani, solo il 52% dei pazienti con febbre presentava gli altri due sintomi indicativi di COVID-19 (tosse e dispnea). Il 38% dei bambini, secondo uno studio italiano pubblicato sul New England Journal of Medicine, ha necessitato di ricovero, 9 dei quali hanno avuto bisogno di supporto respiratorio (6 con patologie preesistenti). Tutti i 100 bambini della casistica risultano guariti.
Questi dati sembrano tranquillizzanti riguardo al COVID-19 pediatrico. Va comunque posta molta attenzione quando a manifestare i sintomi dell’infezione sono i bambini con meno di un anno. Studi eseguiti da scienziati cinesi e pubblicati su Jama su madri in gravidanza con infezione da SARS-CoV-2 hanno indagato la relazione fra immunità materna e protezione del neonato dall’infezione, senza giungere però a risultati conclusivi. Il riscontro quindi, in neonati figli di madre SARS-CoV-2 positive, di sintomi indicativi come febbre, difficoltà respiratoria, tosse, sintomi gastrointestinali e tendenza al sopore, deve allertare i genitori e il pediatra.
Fonte: ISS
 A maggio l’Associazione delle Scuole di Sanità Pubblica nella Regione Europea (ASPHER) ha pubblicato il documento “COME CONTARE I CASI? Concetti epidemiologici di base per comprendere l’epidemia di COVID-19”.
A maggio l’Associazione delle Scuole di Sanità Pubblica nella Regione Europea (ASPHER) ha pubblicato il documento “COME CONTARE I CASI? Concetti epidemiologici di base per comprendere l’epidemia di COVID-19”. La circolazione pandemica di SARS-CoV-2 è legata alla trasmissione da uomo a uomo. Tuttavia, alcune recenti evidenze, sia di natura osservazionale che sperimentale, hanno posto all’attenzione della comunità scientifica e delle autorità sanitarie, il tema della suscettibilità degli animali a SARS-CoV-2.
La circolazione pandemica di SARS-CoV-2 è legata alla trasmissione da uomo a uomo. Tuttavia, alcune recenti evidenze, sia di natura osservazionale che sperimentale, hanno posto all’attenzione della comunità scientifica e delle autorità sanitarie, il tema della suscettibilità degli animali a SARS-CoV-2.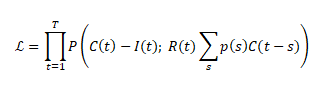
 Si chiama
Si chiama 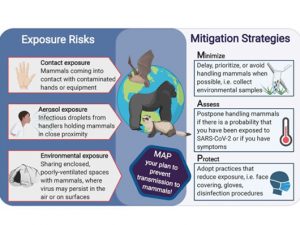 L’Oie, Organizzazione mondiale per la sanità animale ha elaborato delle linee guida rivolte ai lavoratori che operano a contatto con la fauna selvatica, in particolare mammiferi.
L’Oie, Organizzazione mondiale per la sanità animale ha elaborato delle linee guida rivolte ai lavoratori che operano a contatto con la fauna selvatica, in particolare mammiferi. L’Istituto Superiore di sanità ha pubblicato il “Rapporto ISS COVID-19 n. 26/2020 – Indicazioni ad interim sulla gestione e smaltimento di mascherine e guanti monouso provenienti da utilizzo domestico e non domestico. Versione del 18 maggio 2020”
L’Istituto Superiore di sanità ha pubblicato il “Rapporto ISS COVID-19 n. 26/2020 – Indicazioni ad interim sulla gestione e smaltimento di mascherine e guanti monouso provenienti da utilizzo domestico e non domestico. Versione del 18 maggio 2020” L’Istituto Superiore di Sanità ha pubblicato ieri i dati del
L’Istituto Superiore di Sanità ha pubblicato ieri i dati del  Sulla base delle evidenze scientifiche disponibili ad oggi non è dimostrato che i pazienti pediatrici che in passato hanno avuto diagnosi di malattia di Kawasaki siano esposti ad un rischio maggiore rispetto agli altri bambini di contrarre SARS-CoV-2, né di presentare una recidiva di malattia di Kawasaki. Tuttavia, recenti pubblicazioni scientifiche descrivono una sindrome infiammatoria acuta multisistemica in età pediatrica e adolescenziale, associata a positività per il SARS-CoV-2 o presenza di anticorpi anti SARS-CoV-2. Questa sindrome sembrerebbe condividere alcune caratteristiche cliniche con la malattia di Kawasaki ma, secondo le indicazioni dell’European Centre for Disease Prevention and Control (ECDC) e della World Health Organization (WHO), si tratta di una forma clinica che va differenziata dalla malattia di Kawasaki e che è ancora in via di definizione.
Sulla base delle evidenze scientifiche disponibili ad oggi non è dimostrato che i pazienti pediatrici che in passato hanno avuto diagnosi di malattia di Kawasaki siano esposti ad un rischio maggiore rispetto agli altri bambini di contrarre SARS-CoV-2, né di presentare una recidiva di malattia di Kawasaki. Tuttavia, recenti pubblicazioni scientifiche descrivono una sindrome infiammatoria acuta multisistemica in età pediatrica e adolescenziale, associata a positività per il SARS-CoV-2 o presenza di anticorpi anti SARS-CoV-2. Questa sindrome sembrerebbe condividere alcune caratteristiche cliniche con la malattia di Kawasaki ma, secondo le indicazioni dell’European Centre for Disease Prevention and Control (ECDC) e della World Health Organization (WHO), si tratta di una forma clinica che va differenziata dalla malattia di Kawasaki e che è ancora in via di definizione.